La spettroscopia si occupa dell'esame e dell'interpretazione degli spettri e delle molecole allorché la materia viene opportunamente eccitata. Uno spettro rappresenta un insieme di radiazioni, emesse o assorbite dagli atomi o dalle molecole, distribuite ed espresse in funzione delle lunghezze d'onda o delle frequenze. L'intero spettro elettromagnetico viene in genere suddiviso in alcune zone che comprendono quelle componenti che all'incirca presentano le stesse caratteristiche di produzione e di rivelazione.
Ci occuperemo dello spettro riguardante la regione del visibile, ossia delle radiazioni corrispondenti all'intervallo di lunghezze d'onda più o meno comprese tra 400 e 700 nm (nanometri) nel vuoto.

Lo studio spettroscopico dell'emissione e dell'assorbimento della luce da parte degli elementi è stato uno dei campi di ricerca fondamentali per lo sviluppo delle conoscenze sulla struttura atomica della materia.
Storicamente questa disciplina ebbe la sua origine allorché Newton mise sperimentalmente in evidenza la scomposizione della luce bianca nelle componenti monocromatiche per mezzo di un prisma trasparente.

Solamente dopo il 1850 la spettroscopia diventò una branca ufficiale della ricerca scientifica; ciò avvenne quando Bunsen e Kirchhoff notarono che la frequenza delle righe spettrali, già osservate e classificate da Fraunhofer negli spettri ottici, poteva caratterizzare la natura chimica degli elementi.
Mediante l'analisi spettroscopica i due ricercatori tedeschi non solo scoprirono nuovi elementi (il rubidio e il cesio), ma indicarono la metodologia per studiare la composizione chimica della materia extraterrestre accessibile all'indagine umana attraverso le radiazioni inviate dalle stelle.
Il primo importante risultato, dedotto dallo studio della luce omessa dai corpi celesti, è rappresentato dalla scoperta, fatta da Lockyer nella radiazione solare, di alcune righe spettrali prodotte ara un elemento ancora sconosciuto sulla Terra. Questo elemento, contenuto inizialmente presente solo nel Sole e pertanto chiamato elio (Hélios = Sole), venne successivamente trovato da Ramsay fiche sul nostro pianeta.
Gli spettri, di solito vengono classificati in:
- spettri di emissione,
- spettri di assorbimento.
A loro volta, sia quelli dell'uno sia quelli dell'altro tipo si dividono in:
- spettri continui,
- spettri di righe,
- spettri di bande.
Spettro di emissione

Lo spettro di emissione si ha quando le radiazioni ottiche emesse da una sorgente opportunamente eccitata vengono direttamente disperse nelle componenti monocromatiche mediante lo spettroscopio, chiamato anche spettrometro se munito di una scala graduata da utilizzare per la misura della lunghezza d'onda della radiazione.
A seconda della materia eccitata si può ottenere:
- uno spettro continuo, se è formato da un insieme, più o meno esteso, di lunghezze d'onda. Nel campo del visibile si presenta con una successione continua di colori che dal rosso si estendono fino al violetto. Viene emesso soprattutto dalla materia in fase solida o in fase liquida quando si riscalda fortemente;
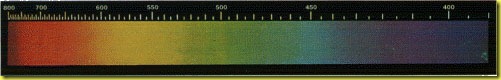
- uno spettro di righe, se è formato da una sequenza discontinua, più o meno numerosa, di righe brillanti e ben separate sopra un fondo scuro. Indipendentemente dalla tecnologia di eccitazione, ogni atomo di un elemento portato allo stato aeriforme presenta uno spettro di righe che caratterizza la natura della materia emittente;
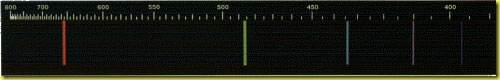
- uno spettro di bande, se è formato da una successione assai fitta di righe che si addensano in corrispondenza di certe lunghezze d'onda. È originato soprattutto dai gas e dai vapori caratterizzati da molecole poliatomiche i cui atomi sono chimicamente legati.

Spettro di assorbimento

Questo tipo di spettro si ottiene interponendo sul cammino della radiazione in grado di originare uno spettro continuo una sostanza, in genere un gas o un vapore, che assorbe, in corrispondenza di certe lunghezze d'onda più o meno estese, alcune componenti che l'attraversano. Si origina così una specie di arcobaleno, sovrapposto al quale le variopinte righe che caratterizzano in emissione la sostanza in fase aeriforme si trasformano, in assorbimento, in una sequenza di righe scure localizzate nella stessa posizione (frequenza) delle prime.
Spettro atomico
Poiché mediante l'analisi spettrale è possibile individuare l'elemento eccitato, la frequenza o la lunghezza d'onda delle righe spettrali rappresentano una caratteristica fondamentale dell'elemento emittente. Per esempio, l'idrogeno emette una serie di righe aventi sempre la stessa lunghezza d'onda, il sodio un'altra successione, il magnesio ancora un'altra, e così via. Non esistono spettri comuni a due elementi distinti. È pur vero che uno stesso elemento può emettere spettri diversi (righe che appaiono, mentre altre scompaiono), ma ciò deriva dalla modalità e dal grado di eccitazione. Comunque, ogni spettro di righe è sempre caratteristico dell'elemento in quelle condizioni di eccitazione.
Per mezzo della spettroscopia si può pertanto fare l'analisi degli elementi, nel senso di riconoscere la presenza di un elemento in un miscuglio di più altri.
Rispetto alle tradizionali metodologie chimiche, questo tipo di analisi possiede il vantaggio di poter utilizzare piccolissime quantità di materia. In genere, per riconoscere la presenza di un elemento non è necessario identificare tutte le righe del suo spettro: basta infatti evidenziare alcune delle sue righe più intense per caratterizzare l'elemento in esame.
Per mezzo dell'analisi spettroscopica è possibile riconoscere oltre agli elementi chimici, caratterizzati da spettri a righe, anche certi composti chimici condotti in fase aeriforme che presentano uno spettro a bande.
Confrontando gli spettri in emissione e in assorbimento, forniti da una stessa sostanza allo stato aeriforme, si nota una corrispondenza, rilevata per la prima volta da Kirchhoff, comunemente chiamata principio d'inversione dello spettro: ogni sostanza aeriforme è infatti capace di assorbire quelle radiazioni che nelle stesse condizioni fisiche è anche capace di emettere. A righe brillanti in emissione corrispondono infatti in assorbimento righe scure localizzate sullo sfondo dello spettro luminoso continuo.

Per esempio, la luce proveniente dal Sole presenta uno spetto di assorbimento: sul fondo continuo si notano moltissime righe nere, dette righe di Fraunhofer.
La parte interna del Sole infatti fornisce uno spettro continuo; però, poiché la luce attraversa anche la cromosfera solare e l'atmosfera terrestre, per assorbimento si forma sullo spettro continuo una numerosa successione di righe oscure, le quali permettono di individuare gli elementi aeriformi della cromosfera. Le righe telluriche, a causa dei pochi elementi dell'atmosfera terrestre, sono infatti trascurabili rispetto alle righe solari.
Anche lo spettro a righe della luce emessa da una stella può rivelare, se opportunamente osservato, la natura chimica e l'abbondanza relativa degli elementi che si trovano sulla superficie esterna del corpo celeste.
_____________________











